1. 서론: 철강 재료의 나침반, Fe-Fe₃C계 상태도
철(Fe)에 탄소(C)를 첨가하여 만들어지는 강(Steel)은 인류 문명을 지탱하는 가장 중요한 소재다. 탄소 함량과 온도 변화에 따라 철의 내부 조직이 어떻게 변하는지를 나타낸 ‘Fe-Fe₃C 계 상태도’는 금속 재료의 성질을 결정짓는 절대적인 지표다. 철강이나 재료를 다루는 엔지니어는 이 지도를 이해함으로써 우리는 원하는 강도와 인성을 가진 최적의 재료를 설계할 수 있다.
참고로, FE-C 계 상태도는 조금 더 넓은 의미로 ‘철-탄소 시스템’ 전체를 아우르는 명칭이다. 엄밀히 말해 ‘Fe-C 상태도’는 시멘타이트가 아닌 ‘흑연’이 석출되는 평형 상태(안정 상태도)까지 포함할 수 있는 표현이다. 현장에서 Fe-C 보다 Fe-Fe₃C 준안정상태도가 더 널리 활용되는 이유는, 실제 강에서 Fe₃C로부터의 흑연화가 거의 발생하지 않기 때문이며, 주철의 경우 흑연화를 촉진하므로 Fe-C 상태도가 바람직하다.
2. 본론: Fe-Fe₃C 상태도의 핵심 메커니즘 분석
(1) 철강의 변태 (Transformation)와 Fe-Fe₃C 상태도내 3대 불변반응
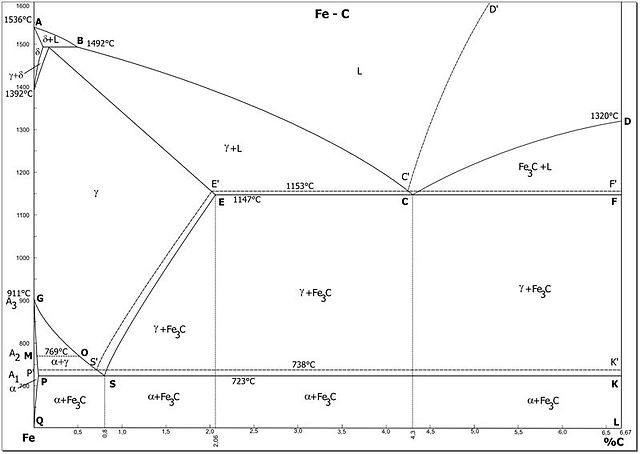
Fe-Fe₃C 상태도, 이미지 출처: Wikimedia Commons (Public Domain)
a. 철강의 변태
Fe-Fe₃C 상태도상에서 철은 온도에 따라 원자 배열이 바뀌는 동소변태와 자기적 성질이 변하는 자기변태를 일으킨다.
- A₁ 변태 (723°C): 공석 변태점이다. 오스테나이트가 펄라이트로 변하는 지점으로, 강(Steel)의 열처리에서 가장 중요한 기준이 된다.
- A₂ 변태 (768°C): 퀴리점(Curie Point)이라 불리는 자기 변태점이다. 강자성체인 철이 이 온도 이상에서 상자성체로 변한다.
- A₃ 변태: 아공석강에서 페라이트가 오스테나이트로 변태하기 시작하거나 끝나는 지점이다.
- A₄ 변태 (1,394°C): 감마(γ)철이 델타(δ)철로 바뀌는 동소 변태점이다.
- A0 변태 (210°C): 강(Steel) 조직 중 하나인 시멘타이트(Fe3C)의 자기 변태(Magnetic Transformation)를 의미한다. 210°C 이하에서 시멘타이트는 자석에 붙는 강자성체 성질을 띠지만, 이 온도를 넘어서는 순간 자성을 잃고 상자성체로 변한다. A2 변태(철의 자기 변태)와 마찬가지로 결정 구조 자체는 바뀌지 않고 오직 자기적 성질만 변하는 변태다. 따라서 상태도 상에서는 수평선으로 나타나며, 금속의 외형이나 결정 격자에는 변화가 없다.
| 변태점 | 온도(약) | 내용 | 비고 |
| A0 | 210°C | 시멘타이트(Fe3C)의 자기 변태 | 강자성 -> 상자성 |
| A1 | 723°C | 공석 변태 (오스테나이트 -> 펄라이트) | 결정 구조 변화 |
| A2 | 768°C | 철(Fe)의 자기 변태 (퀴리점) | 강자성 -> 상자성 |
| A3 | 911°C | 동소 변태 (페라이트 -> 오스테나이트) | BCC -> FCC |
| A4 | 1,394°C | 동소 변태 (오스테나이트 -> 델타 페라이트) | FCC -> BCC |
표 : Fe-Fe₃C 상태도 상의 변태점
b. 철의 동소체: α, γ, δ 철의 이해
철은 온도 구간에 따라 결정 구조가 변하며, 이는 탄소의 고용도와 재료의 성질을 결정짓는다.
- α-철 (페라이트, BCC): 상온에서 911°C 사이의 구조다. 원자 배열이 체심입방격자(BCC)로, 탄소가 들어갈 틈새가 적어 탄소 고용도가 매우 낮다(최대 0.022%).
- γ-철 (오스테나이트, FCC): 911°C에서 1,394°C 사이의 구조다. 면심입방격자(FCC)이며, BCC보다 격자 사이의 빈 공간이 커서 탄소를 많이 포함할 수 있다(최대 2.11%). 열처리의 모상이 되는 중요한 조직이다.
- δ-철 (델타 페라이트, BCC): 1,394°C에서 용융점(1,538°C) 사이의 고온 구간이다. α-철과 같은 BCC 구조를 가진다.
- 참고 (β-철): 과거에는 768°C(A₂ 변태점)에서 자기 성질이 변하는 구간을 β철이라 불렀으나, 결정 구조의 변화가 없는 자기 변태이므로 현재는 동소체로 분류하지 않는다.
C. Fe-Fe₃C 상태도의 3대 불변반응
Fe-Fe3C 상태도 상에서 특정 온도와 성분일 때, 자유도가 0이 되어 온도가 일정하게 유지되는 구간을 불변반응이라 한다.
- 포정 반응 (Peritectic Reaction, 1,495°C):
- 반응식: Liquid + δ(BCC) -> γ(FCC)
- 고온의 액체와 고체(δ)가 만나 새로운 고체(γ)를 형성하는 반응이다. 탄소 함량 약 0.17% 부근에서 일어난다.
- 공정 반응 (Eutectic Reaction, 1,148°C):
- 반응식: Liquid -> γ(FCC) + Fe3C(Cementite)
- 액체 상태에서 두 개의 고체(오스테나이트와 시멘타이트)가 동시에 석출되는 반응이다. 탄소 함량 4.3%에서 발생하며, 이 조직을 레데부라이트(Ledeburite)라 부른다. 주철(Cast Iron)의 특징을 결정짓는 반응이다.
- 공석 반응 (Eutectoid Reaction, 723°C):
- 반응식: γ(FCC) -> α(BCC) + Fe3C(Cementite)
- 고체(γ)에서 두 개의 고체(페라이트와 시멘타이트)가 층상으로 석출되는 반응이다. 탄소 함량 0.8%에서 발생하며, 이때 형성되는 조직이 바로 펄라이트(Pearlite)다. 강(Steel)의 성질을 조절하는 가장 핵심적인 반응이다.
(2) FCC(오스테나이트) vs BCC(페라이트): 결정 구조와 침입형 자리
철의 동소체인 α-Fe와 γ-Fe의 성질 차이는 원자 배열 방식과 그 사이의 빈 공간인 ‘침입형 자리(Interstitial Site)’의 크기에서 기인한다. 탄소 원자는 철 원자보다 작아 이 빈 공간에 끼어들어 가는 ‘침입형 고용체‘를 형성하기 때문이다.
a. 결정 구조 및 원자 충진율 비교
- BCC (체심입방격자, α-Fe): 입방체의 꼭짓점과 중심에 원자가 위치한다. 원자 충진율은 68%로, FCC보다 원자들이 듬성듬성하게 배열된 것처럼 보이지만, 아이러니하게도 내부의 개별 빈 공간은 매우 작다.
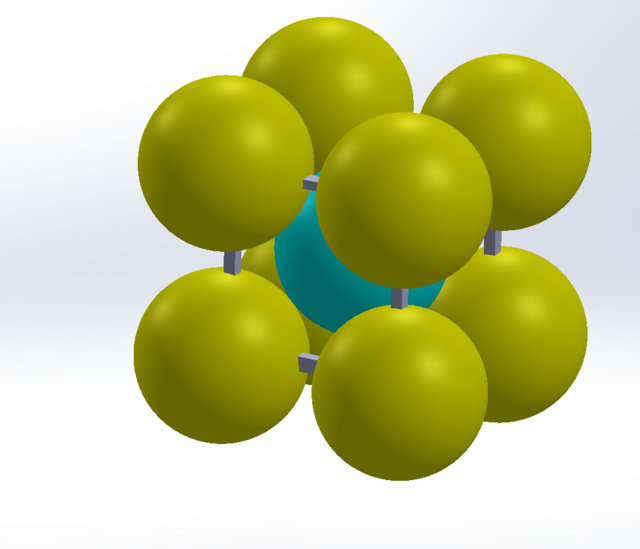
BCC 구조, 이미지 출처: Wikimedia Commons (Public Domain)
- FCC (면심입방격자, γ-Fe): 입방체의 꼭짓점과 각 면의 중심에 원자가 위치한다. 원자 충진율은 74%로 원자들이 매우 조밀하게 쌓여 있으나, 그 사이사이에 존재하는 빈 공간의 크기는 BCC보다 크다.
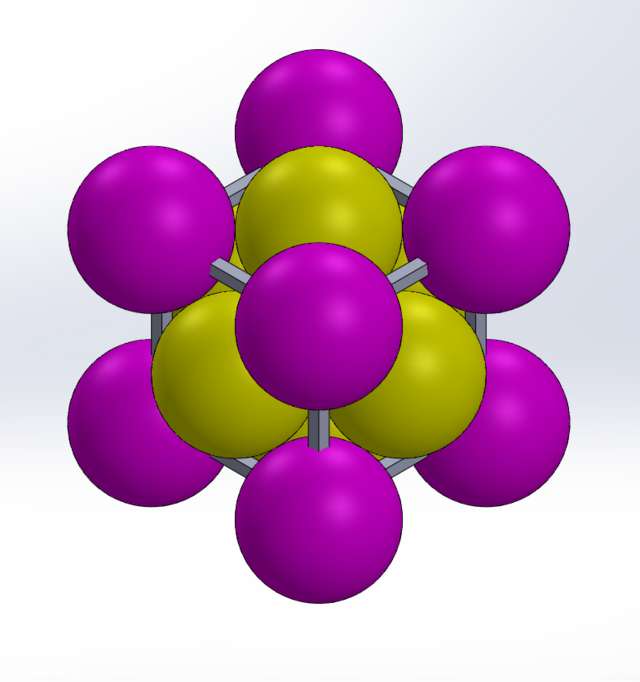
FCC 구조, 이미지 출처: Wikimedia Commons (Public Domain)
b. 침입형 자리(Interstitial Site)의 비교 분석
탄소(C) 원자가 들어갈 수 있는 자리는 크게 팔면체 자리(Octahedral site)와 사면체 자리(Tetrahedral site)로 나뉜다.
- BCC의 침입형 자리 (매우 협소):
- BCC 구조 내에서 가장 큰 빈 공간은 팔면체 자리지만, 그 모양이 찌그러진 형태다.
- 철 원자 사이의 간격이 너무 좁아 탄소 원자(반경 약 0.77Å)가 들어가기에 공간이 턱없이 부족하다(BCC 팔면체 자리 반경 약 0.19Å).
- 이 때문에 탄소는 BCC 구조에 거의 녹아 들어가지 못하며, 최대 고용도가 0.022%에 불과하다.
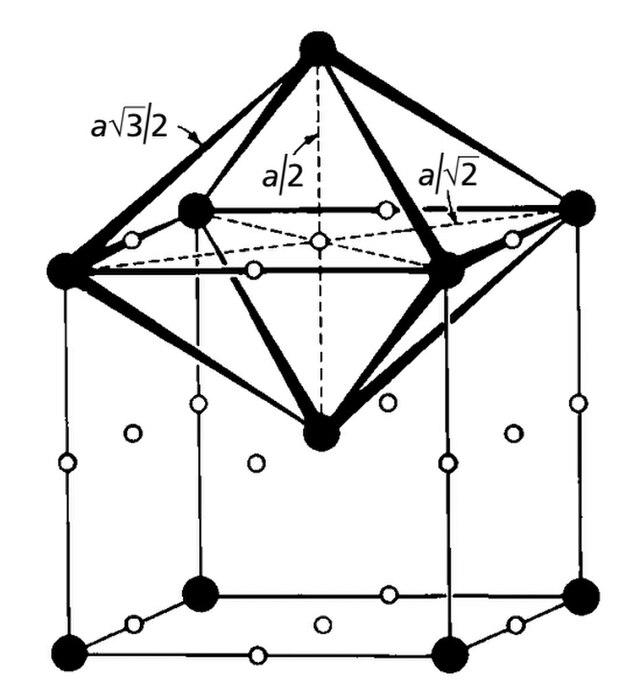
BCC 구조 8면체 자리, 이미지 출처: Wikimedia Commons (Public Domain)
- FCC의 침입형 자리 (상대적 여유):
- FCC 구조의 팔면체 자리는 BCC보다 훨씬 크고 대칭적인 공간을 제공한다.
- 철 원자들이 조밀하게 쌓여 있음에도 불구하고, 그 중심에 형성되는 빈 공간의 크기가 탄소 원자를 수용하기에 훨씬 유리하다(FCC 팔면체 자리 반경 약 0.52Å).
- 이 덕분에 탄소 고용도가 최대 2.11%까지 비약적으로 상승한다.
c. 공학적 시사점: 열처리의 근본 원리
이 구조적 차이가 바로 ‘담금질(Quenching)’의 원동력이 된다.
- 고온의 FCC(오스테나이트) 상태에서 탄소를 듬뿍 녹여둔다.
- 이를 급냉시키면 철은 BCC 구조로 돌아가려 하지만, 이미 녹아 있는 탄소들이 공간이 좁아진 BCC 내부에서 빠져나오지 못하고 갇히게 된다.
- 이 과정에서 격자가 심하게 뒤틀리며 형성되는 조직이 바로 초고경도의 마르텐자이트(Martensite)다.
(3) 탄소 함량에 따른 조직의 변화와 상분율의 역학
탄소강의 기계적 성질은 페라이트(α)와 시멘타이트(Fe3C)라는 두 상의 분포 상태에 의해 결정된다. 특히 공석점(0.8% C)을 기준으로 조직의 구성과 비율이 급격히 변한다.
a. 탄소 함량에 따른 조직의 분류 및 특성
탄소 함량에 따라 강과 주철이 분류되는데, 탄소함량이 보통 2.1% 이내이면 강이되고, 이상이면 주철이 된다. (이사이트 내 글 [금속재료_주철1] 주철(Cast Iron)의 이해 (종류와 특성): 철과 강의 차이는? 참조) 그리고 강내에서는 탄소함량 0.8% 기준으로 아공석강과 과공석강으로 분류할 수 있다.
- 아공석강 (Hypo-eutectoid Steel, C < 0.8%):
- 냉각 시 오스테나이트에서 선공석 페라이트가 먼저 석출된 후, 나머지 오스테나이트가 펄라이트로 변태한다.
- 조직: 페라이트(연성) + 펄라이트(강도). 탄소량이 적을수록 페라이트 면적이 넓어 부드럽고 전성이 좋다.
- 공석강 (Eutectoid Steel, C = 0.8%):
- 723°C(A₁ 점)에서 모든 오스테나이트가 동시에 페라이트와 시멘타이트의 층상 구조인 펄라이트로 변한다.
- 조직: 100% 펄라이트. 층상 구조 특유의 균형 잡힌 강도와 인성을 지닌다.

펄라이트 층상구조, 이미지 출처: Wikimedia Commons (Public Domain)
- 과공석강 (Hyper-eutectoid Steel, C > 0.8%):
- 오스테나이트 결정 입계에 선공석 시멘타이트가 망상(Network) 구조로 먼저 석출된 후 펄라이트가 형성된다.
- 조직: 펄라이트 + 시멘타이트(경도). 매우 단단하지만 취성이 커져 잘 깨지는 성질을 갖는다.
b. 상분율의 계산: 지레대 원리 (Lever Rule)
특정 온도와 농도에서 각 상이 차지하는 무게 비율(상분율)은 상태도상의 선분을 이용한 ‘지레대 원리’로 계산한다.
- 계산 원리: 평형 상태에서 전체 합금의 탄소 농도를 Co, 두 상의 농도를 각각 Cα, Cβ라 할 때, 한 상의 비율은 반대편 선분의 길이에 비례한다. Wα = (Cβ – Co)/(Cβ – Cα)
- 공석 온도(723°C) 직후 펄라이트 내 상분율:
- 펄라이트는 0.022% C의 페라이트와 6.67% C의 시멘타이트로 구성된다.
- 전체 탄소량이 0.8%인 공석강의 경우, 시멘타이트의 비율은 약 12%{(0.8-0.022)/(6.67-0.022)}, 페라이트의 비율은 약 88%가 된다.
- 이 12%의 아주 단단한 시멘타이트 층이 88%의 부드러운 페라이트 사이사이에 끼어 있어 강의 강도를 지탱하는 것이다.
c. 공학적 시사점: 상분율 조절과 재료 설계
- 강도 제어: 탄소 함량을 높이면 시멘타이트의 상분율이 증가하여 강도와 경도가 상승한다.
- 결정립 미세화: 냉각 속도를 조절하여 펄라이트 층 사이의 간격(Interlamellar spacing)을 좁히면, 상분율이 같더라도 훨씬 강한 재료를 얻을 수 있다.
- 불순물의 영향: 실제 현장에서는 황(S)이나 인(P) 같은 불순물이 상분율의 평형을 깨뜨리거나 입계에 편석되어 취성을 일으키므로 엄격한 제어가 필요하다.

Fe-Fe₃C계 상태도, 이미지 출처: Wikimedia Commons (Public Domain)
(4) Fe-Fe₃C계 상태도에 미치는 합금원소의 영향
합금원소의 첨가는 Fe-Fe₃C 상태도의 변태점(A1, A3) 위치와 공석점의 탄소 농도를 변화시켜, 열처리 조건과 최종 조직의 성질을 근본적으로 바꾼다.
a. Fe-Fe₃C계 상태도의 변화: 오스테나이트 vs 페라이트 안정화
합금원소는 크게 두 가지 그룹으로 나뉘어 Fe-Fe₃C 상태도의 영역을 확장하거나 축소시킨다.
- 오스테나이트 안정화 원소 (Ni, Mn, Co, C, N): A3 변태점을 낮추어 오스테나이트(γ) 구역을 확장한다.
- 특히 니켈(Ni)이나 망간(Mn)을 대량 첨가하면 상온에서도 오스테나이트 조직을 유지하는 ‘스테인리스강’ 등을 만들 수 있다.
- 페라이트 안정화 원소 (Cr, Mo, W, V, Si, Al): A3 변태점을 높이고 A4 변태점을 낮추어 오스테나이트 구역을 축소시킨다(Gamma Loop 형성).
- 고온에서도 페라이트 구조를 안정화하여 내열성을 높이는 역할을 한다.
b. 강의 5대 원소의 역할과 영향
강의 제조 과정에서 불가피하게 포함되거나 의도적으로 조절되는 C, Si, Mn, P, S는 Fe-Fe₃C계 상태도와 기계적 성질에 결정적인 영향을 미친다.
- 탄소 (C): 강도의 핵심. 함량이 증가할수록 공석 온도(A1)를 낮추고 시멘타이트 상분율을 높여 경도를 상승시킨다.
- 규소 (Si): 강한 페라이트 안정화 원소다. A3 점을 높이며, 결정립을 조대화시키는 경향이 있으나 전자기적 특성을 개선하고 인장강도를 높인다.
- 망간 (Mn): 오스테나이트 안정화 원소다. A1 변태 온도를 낮추고 소입성(Hardenability, 담금질 효과)을 획기적으로 개선한다. 또한 황(S)과 결합하여 MnS를 형성함으로써 황에 의한 고온 취성을 방지한다.
- 인 (P): 상온 취성(Cold Shortness)의 주범이다. 페라이트에 고용되어 강도를 약간 높이기도 하지만, 결정립계에 편석되어 충격 저항을 급격히 떨어뜨리므로 극히 소량으로 제한해야 한다.
- 황 (S): 고온 취성(Hot Shortness)의 원인이다. 철과 결합해 용융점이 낮은 FeS를 형성하여 압연 등 고온 가공 시 재료를 갈라지게 만든다. 이를 막기 위해 반드시 망간(Mn)과 세트로 관리한다.
c. 공석점(Eutectoid Point)의 이동
대부분의 합금원소(특히 Ti, Mo, W, Cr, Mn, Ni)는 Fe-Fe3C 상태도에서 공석 반응이 일어나는 탄소 농도(0.8% C)를 왼쪽(저탄소 방향)으로 이동시킨다.
공학적 의미: 합금강에서는 탄소 함량이 0.8%보다 훨씬 적어도 전체 조직을 펄라이트(또는 그에 준하는 미세 조직)로 만들 수 있음을 의미하며, 이는 용접성과 강도를 동시에 잡는 핵심 원리가 된다.
3. 결론: 상태도(Fe-Fe₃C) 이해가 가져오는 공학적 혁신
Fe-Fe₃C계 상태도는 단순히 이론적인 도표가 아니라, 담금질, 뜨임, 풀림과 같은 열처리 공정의 설계도와 같다. FCC와 BCC의 구조적 이해와 합금 원소의 영향을 파악함으로써, 우리는 현대 산업이 요구하는 초고장력강이나 특수합금강을 제조할 수 있는 기틀을 마련하게 된다. 결국 금속 재료의 미래는 이 상태도 위의 선들을 얼마나 정밀하게 제어하느냐에 달려 있다.
현장 기술사의 한마디 : 상태도는 ‘평형’ 상태, 즉 아주 천천히 냉각했을 때의 결과다. 하지만 실제 현장(용접이나 퀜칭)은 급랭이 일어나기 때문에 이 지도대로만 흘러가지 않는다. 그래서 우리는 TTT 곡선(항온변태도)을 함께 봐야 한다. 하지만 상태도를 모르면 TTT도 없다. 기초가 없으면 사상누각임을 잊지 말아야 한다.
- 참조자료: 네이버지식백과_평형상태도
ⓒ 2026 Material-Welding-PE.com All rights reserved. 본 콘텐츠의 저작권은 저자에게 있으며, 출처를 밝히지 않은 무단 전재를 금합니다.